|
"Хвойные бореальной зоны" 2003г.,№1, с.
ЭКСТРАКЦИОННАЯ ПЕРЕРАБОТКА КОРЫ ЛИСТВЕННИЦЫ В ПРАКТИЧЕСКИ ПОЛЕЗНЫЕ ПРОДУКТ
Бабкин В.А, Иванова Н.В, Остроухова Л.А, Малков Ю.А, Иванова С.З, Попова О.В.
Иркутский институт химии им. Е.А. Фаворского СО РАН, г.Иркутск
Работа выполнена при финансовой поддержке Минпромнауки России в рамках подпрограммы "Комплексное использование древесного сырья
Предложена схема экстракционной переработки коры лиственницы -многотоннажного отхода деревоперерабатывающей промышленности. Изучены химический состав и свойства получаемых продуктов - воска, антиоксидантного фитокомплекса, водорастворимых веществ, пектиновых веществ и сорбента. Предложены направления их использования.
The scheme of extraction processing of a bark of a larch - large of withdrawal of a wood industry' is offered. Are studied an elemental composition and properties of received products - wax, antioxidant phytocomplex, water-soluble substances, pectic substances and sorbent The directions of their usage are offered
На долю лиственницы, являющейся водорастворимые вещества, пектиновые основной лесообразующей породой лесного вещества и сорбент. фонда России, приходится до 40% Воск по химическому составу представляет нерационально используемого остаточного собой смесь эфиров алифатических кислот с материала. Отличительной особенностью жирными спиртами (С|6-С24) и Р-ситостерином, а лиственницы является толстая кора, отходы также сложных эфиров феруловой кислоты и которой по массе достигают 184 кг/м3 насыщенных длинноцепочечных спиртов (С2[гперерабатываемой древесины. Большая их часть С24), с преимущественным содержанием (по в настоящее время используется в качестве данным ГЖХ) докозанола (С22). Особенно топлива. Однако известно [1], что по своему интересно наличие в лиственничном воске химическому составу кора лиственницы является алкилферулатов, что объясняется наличием
перспективным сырьем для получения ряда широкого спектра биологической активности у
практически ценных продуктов. самой феруловой кислоты и ее производных, на
Целью настоящей работы явилось: основе которых запатентовано много
1.Разработка схемы экстракционной лекарственных и косметических средств [6,7].
переработки коры лиственницы Согласно гигиеническому заключению [3]
- Определение химического состава по органолептическим, физико-химическим, получаемых продуктов радиологическим, токсикологическим
- Определение направления использования показателям воск из коры лиственницы получаемых продуктов соответствует санитарно-гигиеническим
Известно [1], что, используя растворители с требованиям безопасности, предъявляемому к возрастающей полярностью, мы можем из сырью для косметической и парфюмерной лиственничной коры получить до 35 % промышленности. Он также обладает экстрактивных веществ. В настоящее время мы биоцидными и выраженно гидрофобными разработали схему, согласно которой получаем свойствами, и поэтому может применяться в пять практически ценных продуктов - воск, качестве поверхностных покрытий для защиты антиоксидантный комплекс (АОК), древесины и древесных материалов от вредной.
воздействия влаги, бактерий и грибов.
Мы разработали способ выделения из коры лиственницы фитокомплекса (АОК) [2], который при предварительном тестировании в модельной системе (соевый лецитин в трис-HCl) проявил антиоксидантную активность в 1,5 раза выше, чем дигидрокверцетин (ДКВ).
АОК по химическому составу является смесью мономерных, димерных и полимерных продуктов. Мономеры представлены фенолокислотами и флавоноидами [4,5]. Методом обращенно-фазной ВЭЖХ идентифицированы кислоты: и-оксибензойная, протокатеховая, ванилиновая, сиреневая, л-кумаровая (цис-, трансформы), феруловая (цис-, транс-формы) и кофейная. Флавоноидные соединения представлены мономерными, олигомерными и полимерными продуктами. Среди флавоноидов идентифицированы: флаванонон - нарингенин, флаванонолы - аромодендрин, дигидрокверцетин, флавонолы - кемпферол, кверцетин, изорамнетин, мирицетин, флаван-3-олы - (-)-эпифецелихин, (+)катехин, (-)-эпикатехин, антоцианидин листвинидин. В составе комплекса обнаружены спиробифлавоноидные соединения (до 10 масс. %), один из которых - лиственол был идентифицирован в коре лиственницы Гмелина ранее [9].
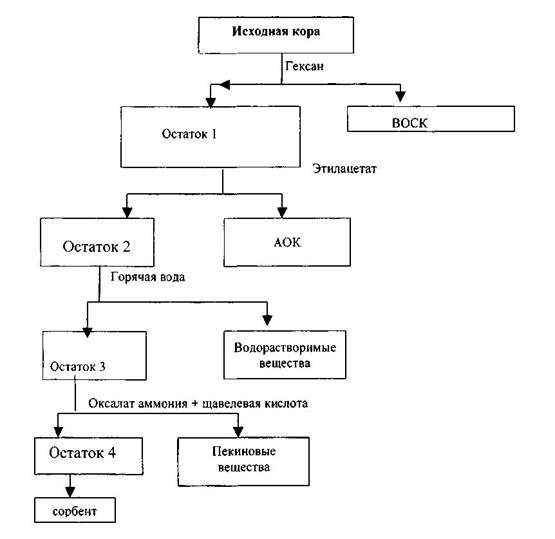
Рисунок 1 - Схема экстракционной переработки коры лиственницы.
Следует отметить, что спиробифлавоноиды это новый класс флавоноидных соединений и к настоящему времени кроме лиственола (синоним лариксинол), известно еще всего четыре соединения: дафнодорин С, выделенный из корней Daphne odora [11], дафнодорины М и N, выделенные из корней и коры Daphne acutiloba [12], и витизинол, выделенный из семян винограда Vitis amurensis Rupr. [13].
Нами в составе антоксидантного комплекса обнаружены еще два спиробифлавоноида, установлением строения которых мы занимаемся в настоящее время.
Хвойные бореальной зоны. 2003. Выпуск 1.
Анализ полимерной фракции АОК методами ИК спектроскопии и спектроскопии ЯМР 13С показал, что по химическому составу она представляет собой продукты конденсации димеров спиро-типа, флаван-3-олов и процианидинов [5].
На основании проведенных в лаборатории фармокологии НИОХ СО РАН токсикофармакологических исследований АОК, было установлено, что он:
-является малотоксичным веществом (IV класс) -оказывает капилляропротекторный эффект
- проявляет гастрозащитные свойства
- - не оказывает влияния на моторноэвакуаторную функцию кишечника
- - проявляет антиоксидантную активность
- - оказывает гепатопротекторный эффект с выраженным антихолестатическим действием
В настоящее время мы ведем работы по созданию на основе АОК новой биологически активной добавки к пище с антиоксидантными, гастрозащитными и гепатопротекторными свойствами. Появление на фармацевтическом рынке России нового фитопрепарата такого типа создаст предпосылки вытеснения дорогостоящих синтетических и природных аналогов зарубежного производства.
Водорастворимые вещества по химическому составу представляют собой смесь мономерных и полимерных продуктов. Последние (до 45% от общего веса фракции) таннины, а мономерная часть представлена
биологически |
активными |
фенолокислотами |
(идентифицированы |
|
л-оксибензойная, |
ванилиновая, |
сиреневая, |
феруловая) |
и |
флавоноидами (дигидрокверцетин и аромадендрин). Высокое содержание таннинов позволяет на основе этой фракции получать дубильные растворы, а выраженные вяжущие и антисептические свойства фракции могут быть использованы для создания на её основе медицинского препарата - аналога коры дуба.
Кора лиственницы содержит от 1,5 до 12,0 % пектиновых веществ [10]. Пектиновые вещества, обладая хорошими желирующими свойствами, традиционно используются в производстве фруктовых, молочных, десертных продуктов, в фармацевтике и косметической промышленности. В настоящее время Россия испытывает серьёзный недостаток в этом продукте, поскольку традиционные источники и заводы по его выделению после распада СССР оказались за рубежом. Поэтому кору лиственницы можно рассматривать как объект для промышленного производства пектинов.
Мы исследовали классические способы выделения пектиновых веществ в приложении к объекту - кора лиственницы сибирской и даурской [8]. Выяснили, что при использовании в качестве экстрагента эквимолярной смеси щавелевой кислоты и оксалата аммония и в качестве осадителя - ацетона или этилового
спирта, можно получить из коры лиственницы пектин в количестве 2 - 6 % от веса сухой коры с
показателями |
качества, |
соответствующими |
стандартам EEC. |
|
|
|
Проэкстрагированная |
кора |
представляет |
собой высокоэффективный сорбент, не требующий дополнительной активации и пригоден, в частности, для очистки промышленных стоков и объектов, загрязненных нефтепродуктами и фенолами. Сорбционная емкость по метиленовому голубому получаемого сорбента сопоставима с таковой для широко известного энтеросорбента полифепана, и составляет -0,05 грамм на грамм сухого продукта.
Таким образом, предложена схема экстракционной переработки коры лиственницы, на основании которой в настоящее время разрабатывается технология утилизации этого крупнотоннажного отхода. Изучены химический состав и свойства получаемых продуктов, предложены направления их использования.
Библиографический список
- В.А. Бабкин, Л.А. Остроухова и др. Безотходная комплексная переработка биомассы лиственниц сибирской и даурской // Химия в интересах устойчивого развития. - 1997. - №5. стр. 105-115.
- Бабкин В.А., Остроухова Л.А., Иванова Н.В., Малков Ю.А., Иванова С.З., Онучина Н.А. // Фитокомплекс, обладающий антиоксидантной активностью и способ его получения. Патент РФ №2188031.
- Гигиеническое заключение Министерства здравоохранения РФ, Центра Государственного санитарно-эпидемиологического надзора в г. Москве на продукцию, товар № 77.01.12.915 П 308553.10.0 от 19.10.00.
- Иванова Н.В., Остроухова Л.А., Бабкин В.А., Иванова С.З., Попова О.В. Комплекс мономерных фенольных соединений коры лиственницы // Химия растительного сырья.1999.-№4. - с.5-7.
- Иванова С.З., Федорова Т.Е., Иванова Н.В., Федоров СВ., Остроухова Л.А., Малков Ю.А., Бабкин В.А. // Флавоноидные соединение коры лиственницы сибирской и даурской // Химия растительного сырья. - 2003 (в печати)
- Патент №6380 Франция, 1968.
- Патент №1480 Япония, 1972.
- Попова О.В., Иванова Н.В., Галкина С.А., Бабкин В.А. Изучение зависимости выхода пектиновых веществ из коры лиственницы от условий их выделения // Тез. докл. Всероссийских научных чтений с международным участием, посвященные 70-летию со дня рождения чл.-кор. АН СССР М.В. Мохосоева . - Улан-Удэ. - 2002 г. -С.171-172.
- Чумбалов Т.К., Пашинина Л.Т., Лейман З.А. Флавоноиды коры Larix sibirica. // Химия природн. соед. - 1970. - № 6. - С. 763-764.
- Ярцева Н.А., Пермякова Г.В., Степень Р.А. Характеристика пищевых пектинов и коры хвойных пород Сибири // Продовольственные и кормовые ресурсы лесов Сибири". - Красноярск. - 1983. - С. 122-124.
- Baba К., Yoshikawa M, Taniguchi М, Kozawa M. Biflavonoids from Daphne odora. // Phytochemistry. - 1995. - Vol 31. - N 4. - P. 10211026.
- Taniguchi M., Fujiwara A., Baba K., Wang N.-H. Two Biflavonoids from Daphneacutiloba. // Phytochemistry. - 1998. - Vol 49. - N 3.
- P. 863-867.
- Wang J.-N., Hano Y., Nomura Т., Chen Y.-J. Procyanidins from the seeds of Vitis amurensis. // Phytochemistry. - 2000. - Vol 53. - P. 1097-1102
|




